「標準治療が終わったら、もう選択肢はないの?」そのような深刻な場面に直面している方もいらっしゃるのではないでしょうか。
- 「治験」「先進医療」「自由診療」の違いがわからず、何を信じればよいか迷っている
- インターネットで情報を探しても、信頼できるのかどうか判断できない
- 標準治療の次の選択肢を探したくても、知識がなく情報量も膨大で時間だけが過ぎ、途方に暮れている、焦りだけが募っていく
そのような状況の患者さんご本人・ご家族に向けて、この記事を書きました。
私は薬剤師として、医療全般に関する基本的な情報収集やその解釈、判断の方法など、一般的・客観的な立場で情報共有させていただけるのではないかと考え、情報発信を始めました。実際に大切な家族をがんで失いましたが、当時も「根拠のある選択」を求めて情報収集した経験もあります。
この記事では、標準治療後の次の選択肢を、安全性と治癒の可能性のバランスのとれた公的制度を順に検討する「6つのステップ」と、信頼できる医療情報の見極め方を合わせて解説します。治験・先進医療等のの仕組み・探し方に加え、エビデンスの読み方やレッドフラッグの見分け方までまとめております。
この記事を読めば、「次に何をすればよいか」が具体的にわかり、担当医への相談にも自信を持って臨めるようになります。
結論として、最も安全でリスクの低い方法は、
「公的な制度から順番に検討し、担当医に相談する」というサイクルを繰り返しながら、可能な範囲でご自身でも信頼できる情報源で根拠を確認し納得できることです。
次の治療選択肢は「公的制度」から順に検討するのが最もリスクが低い方法です
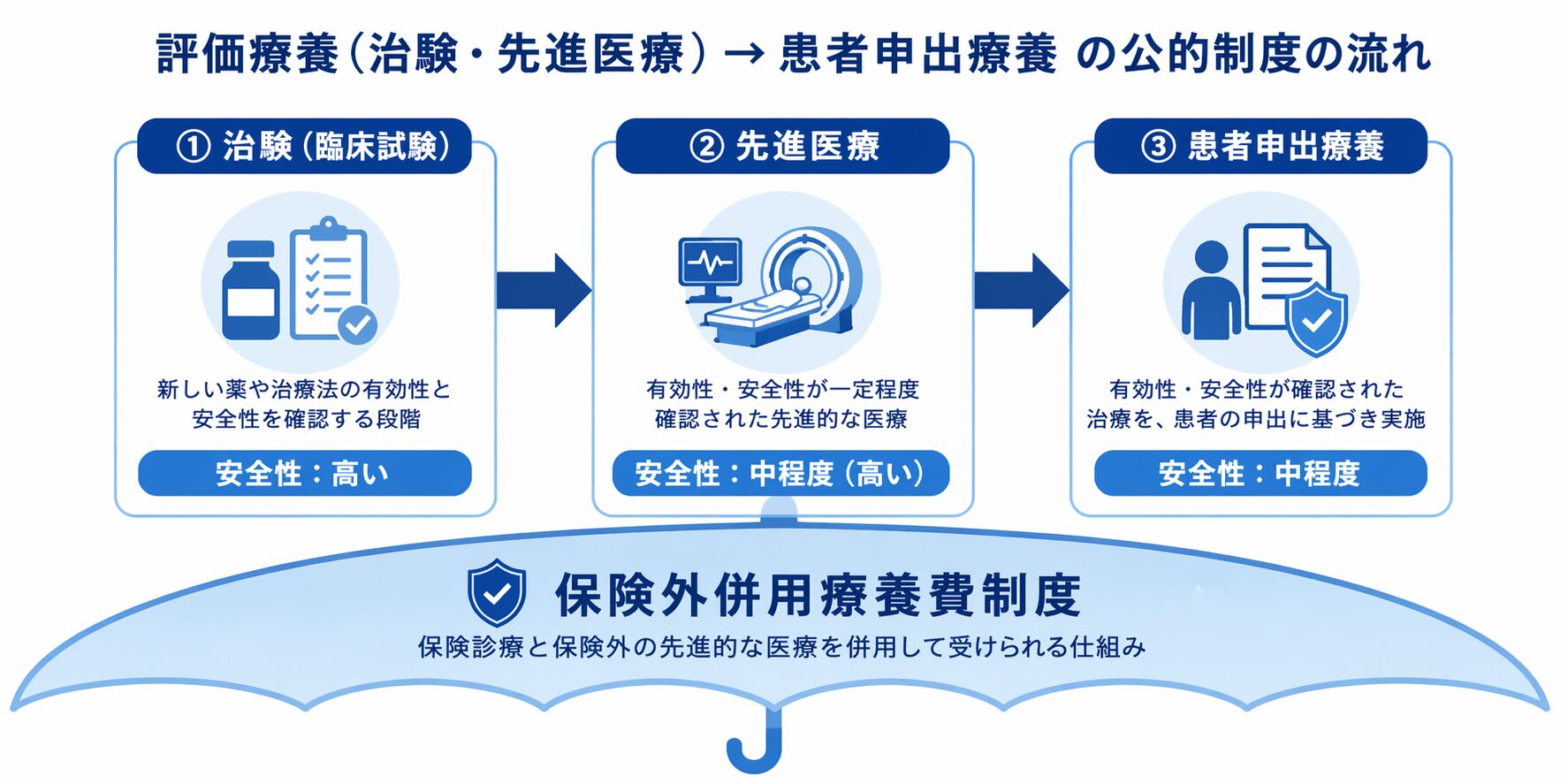
標準治療が奏功しなくなった段階では、治療の検討ステージは「研究段階の医療(治験や先進医療など)」や「エビデンスに基づく補完・統合医療」へと移ります。どちらから検討する場合においても、最初に担当医と話し合うことが大前提です。
公的な制度に基づく選択肢には、国が安全性と有効性を管理しているという共通点があります。一方、自由診療(民間療法)は、審査基準が公的制度に基づくものほど厳格でない場合が多く、効果の保証がないまま多額の費用を支払うリスクが高くなります。
まずは公的制度を順に検討することが、最も効率的で安心できる進め方です。
公的制度 = 保険外併用療養費制度の枠組みで使える制度
まず結論になります。公的制度 = 保険外併用療養費制度の枠組みで使える制度として、
評価療養と患者申出療養を検討していくと良いと考えられます。
研究段階の医療のうち、
評価療養は、厚生労働大臣が保険診療とすべきかどうかの評価が必要であると定めた治療法のことを指し、治験や先進医療がこれに該当します。
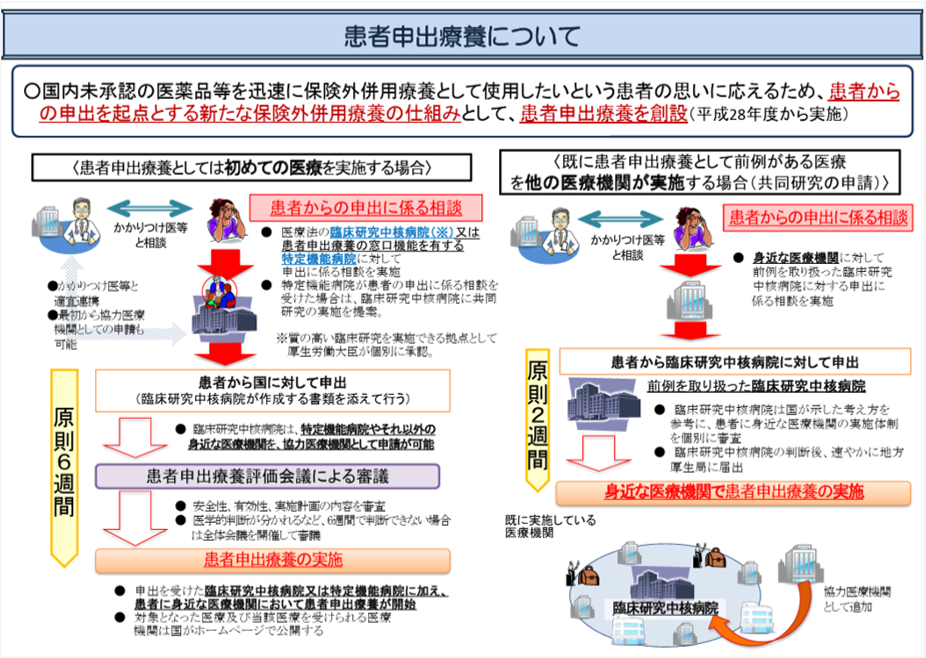
患者申出療養は、患者の申出を起点とし、国において安全性・有効性等を確認し、身近な医療機関で迅速に受けられるようにするものを指します。
これらに共通する点として、
保険診療として認められていないものの、将来的に保険診療となることを目指すものである点です。
(引用元:保険外併用療養費制度についてー厚生労働省)
(引用元:2.研究段階の医療に関する制度について~保険外併用療養費制度ーがん情報サービス)
| 評価療養 | 企業治験 主たる治験 拡大治験 医師主導治験 先進医療A・B |
保険収載を前提に評価を 行うもの |
|---|---|---|
| 患者申出療養 | 患者申出療養 | |
| 選定療養 | 特別の療養環境(差額ベッド)など※ | 保険収載を前提としないもの |
「保険外併用療養費制度」について理解する
「保険外併用療養費制度」とは、研究段階の医療(治験や先進医療など)に関する医療費について、研究段階の医療行為そのものの費用は自己負担となりますが、研究段階の医療以外の費用は保険適用となります。この制度が「保険外併用療養費制度」です。
前述の通り、評価療養(治験・先進医療)および患者申出療養などの医療費について、
研究段階の医療の費用は自己負担となりますが、研究段階の医療以外の費用は保険適用となります。この制度が「保険外併用療養費制度」です。
これは保険診療(すでに保険診療として認められている診察や検査、入院料などにかかる費用など)と保険診療外(研究のために行われる検査や使用される試験薬など)を組み合わせて受けられる仕組み(混合診療の例外的な容認)に伴うものです。
保険外併用療養費制度
- 国民皆保険の理念の下、保険診療と保険外診療の併用(いわゆる混合診療)は原則として禁止されています。それは、混合診療を制限なく許してしまうと、安全性や有効性がまったく確認されていない医療を保険外診療として行うことを助長するおそれがあるからです。(一部抜粋)
- 研究段階の医療では、保険診療として認められていないものの、将来的に保険診療となることを目指すものであることから、安全性や有効性を確認するなどの一定のルールの下で保険診療との併用ができるよう、保険外併用療養費制度として、いくつかの公的な制度が設けられています。(引用元:2.研究段階の医療に関する制度について~保険外併用療養費制度)
なお、
保険診療(研究段階の医療以外)の費用の患者部分については高額療養費制度を活用でき、
保険診療外(研究段階の医療)の費用については所得税の医療費控除を受けることができます。
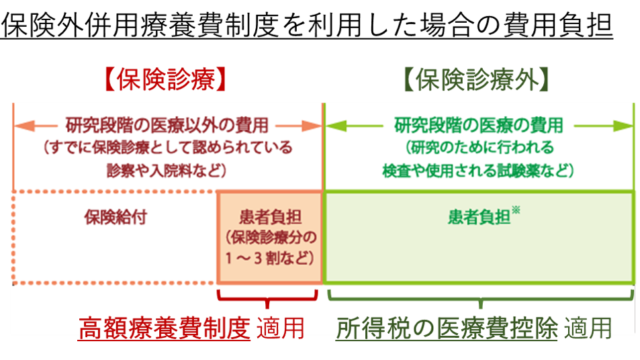
(引用元:3.研究段階の医療にかかる費用負担より一部改変)
制度の枠組みを理解しておくことで、「どの部分にいくらかかるか」を事前に整理しやすくなります。
臨床試験・臨床試験以外の枠組み
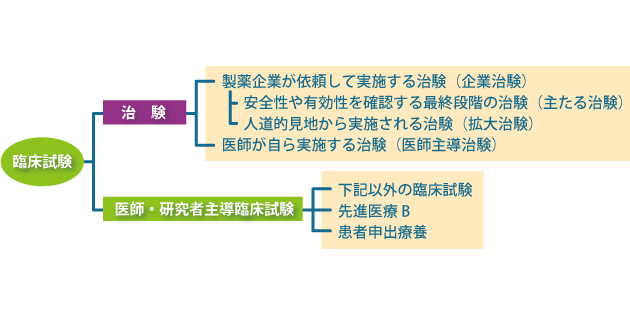
(引用元:臨床試験の種類ーがん情報サービス)
ここで今一度整理しておきましょう。
臨床試験
「新しい薬や技術を使い、特別な観察を必要とする(人体への介入となる)試験」
- まだ日本で認められていない薬(未承認薬)や、別の病気のために認められた薬(適応外薬)をメインに使用
- 人の体に変化を起こさせる「介入」を行うため、副作用がないか、本当に効果があるかを「特に重点的に観察・評価」する必要がある
- 治験(企業治験・主たる治験・拡大治験・医師主導治験・医師・研究者主導臨床試験)、
先進医療B、患者申出療養など
〈例外〉承認済みの薬同士の「より良い組み合わせ」や「新しい使い方」を試すような
研究的な側面が強い場合 = 医師・研究者主導臨床試験
(未承認薬等の使用が「無し」であっても、人体への変化を伴う「介入」となり臨床試験の枠組みで実施される場合がある)
臨床試験以外
「既に一定の安全性が判明されている技術を使い、特別な観察を必要としない(人体への影響が小さい)試験」
- 原則として未承認薬や適応外薬を使用しない
- すでに国内で使われている薬や技術が中心であるため、臨床試験のような「特に重点的な観察」を必要としないと判断されたもの
- 先進医療Aや、薬事承認後で保険収載待ちの薬の使用など
〈例外〉未承認の検査薬や体外診断薬 = 先進医療Aなど
(人体への影響が極めて小さいものであれば、先進医療Aに含まれる場合がある)
参考までに以下のような考え方も添えさせていただきます。(あくまで個人的な主観の域を出ません。)
- 「新しい薬」に期待するなら「臨床試験」
まだ世に出ていない最新の薬を試したい場合は、治験や先進医療B、患者申出療養といった「臨床試験」の枠組みに参加することになります。これらは安全性を確かめる「試験」であるため、検査や診察が非常に細かく行われます。 - 「既存の技術」を受けるなら「臨床試験以外の枠組み」
未承認薬を使わない「先進医療A」などは、試験というよりも「保険適用を待っている治療」に近い感覚かと思います。臨床試験ほどの過密なスケジュールでの観察は求められないのが一般的です。
また、用語の意味、および各臨床試験等の比較表を以下にまとめました。
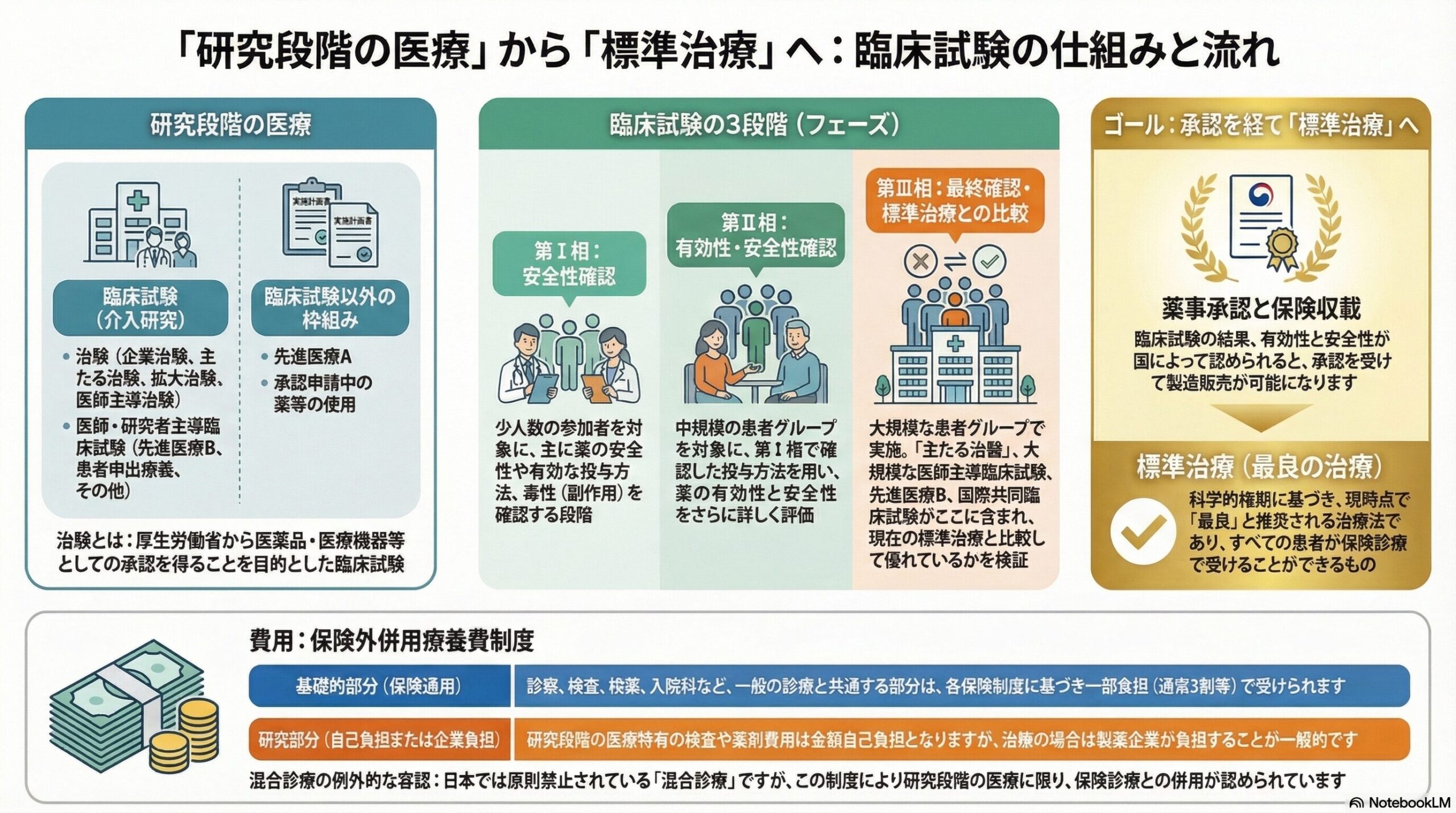
- 研究段階の医療:よりよい標準治療の確立を目指している研究・開発中の医療
- 臨床試験:薬の投与、手術、放射線治療などにより、人体に対して変化を伴う介入研究
- 介入研究:対象者に対して何らかの変化を起こさせ、その結果どのように変化
したかを評価する研究 - 評価療養:厚生労働大臣が保険診療とすべきかどうかの評価が必要であると定めた治療法で、保険外併用療養費制度の中で保険診療との併用が認められている療養
- 治験:医薬品医療機器等法に従い、未承認薬や適応外薬、新しい医療機器等に対して、厚生労働省から医薬品・医療機器等としての承認を得ることを目的として行う臨床試験
(その多くは薬を開発している製薬企業等が医師に依頼をして実施される企業治験) - 主たる治験:効能・効果および用法・用量が一連の開発を通じて設定された後、安全性や有効性を確認する最終段階のもの
- 拡大治験:必要な薬の承認および保険適用までの期間を待つことができない生命に重大な影響がある疾患をもち、既存の治療法に有効なものが存在せず、新しい薬などを検討するにあたり、企業治験や医師主導治験の対象とならない患者さんに対して、
主たる治験の実施は終了したがまだ承認されていない、あるいは実施中(被験者が試験参加中で募集は終了している)の治験薬で行う試験 - 医師主導治験:製薬企業の採算性などの理由で開発がされず、海外では承認されていながら国内では承認されていない、あるいは、その疾患に対しては使用が認められないままになってしまう薬に対し、医療上の必要性に基づき、企業ではなく医師が実施する治験
- 先進医療A:先進医療Aは臨床試験以外の枠組みで評価中のもので、未承認薬等を用いない治療法、または人体への影響が極めて少ない未承認薬等を用いる診断法が該当
(医療技術ごとに一定の施設基準を満たしていることを厚生労働大臣に認められた医療機関でのみ利用可能) - 先進医療B:未承認の治療法を含む、または未承認の治療法を含まない場合でも臨床試験として、安全性および有効性の評価が特に必要とされる治療法
(医療技術ごとに一定の施設基準を満たしていることを厚生労働大臣に認められた医療機関でのみ利用可能) - 医師・研究者主導臨床試験:医師や研究者が主体となって行い、これまで厚生労働省で承認された薬、治療法や診断法から、最良の方法や薬のよりよい組み合わせを確立することを目的として行う試験
(希少なケースとして、未承認薬を用いる場合で企業が利益を見込めず承認申請を行わないが、学術的な関心から初期段階の効果を探索する試験) - 患者申出療養:未承認薬などを必要とする困難な病気と闘う患者さんからの申出により実施されるもので、欧米での承認があるなど、一定の安全性および有効性(科学的根拠)が確認された治療法が対象
(他の研究段階の医療では実施されていないような医療について、将来的に保険収載につなげるための科学的根拠を集積するため) - 国際共同治験:新薬の世界規模での開発・承認を目指して企画される治験であって、一つの治験に複数の国又は地域の医療機関が参加し、共通の治験実施計画書に基づき、同時並行的に進行する臨床試験。主に第Ⅲ相試験が対象とされている。
| 〈各臨床試験等の比較表〉 | |||||||
|---|---|---|---|---|---|---|---|
| イメージによる分類 | 枠組み | 種類 | 未承認薬/機器適応外薬の使用 | 新しい医療技術(手術・手技)の評価 | 主体 | 公的制度 | |
| 研究段階の医療以外(基礎的部分)への保険適用 (保険外併用療養費制度) |
研究段階の医療(上乗せ部分)の費用 (研究のために行われる検査や試験期間中に使用される試験薬など) |
||||||
| 新薬・新機器の国からの承認を目指す試験 | 臨床試験 | 企業治験 | あり | なし | 製薬企業 | 評価療養 | 患者負担なし※5 |
| 新薬・新機器の国からの承認を目指す試験 | 臨床試験 | 主たる治験 | あり | なし | 製薬企業 | 評価療養 | 患者負担なし※5 |
| 新薬・新機器の国からの承認を目指す試験 | 臨床試験 | 拡大治験 | あり | なし | 製薬企業 | 評価療養 | 試験により患者負担あり |
| 新薬・新機器の国からの承認を目指す試験 | 臨床試験 | 医師主導治験 | あり | なし | 医師 | 評価療養 | 試験により患者負担あり |
| 保険適用を目指す試験 | 臨床試験以外 | 先進医療A | なし※1 | あり | 医療機関 | 評価療養※3 | 患者負担あり |
| 保険適用を目指す試験 | 臨床試験 | 先進医療B | あり※2 | あり | 医師・研究者 | 評価療養 | 試験により患者負担あり※6 |
| 保険適用を目指す試験 | 臨床試験 | 患者申出療養 | あり | あり | 患者 → 医師・研究者 | 患者申出療養 | 患者負担あり |
| 最良の使い方を確立する試験 | 臨床試験 | 医師・研究者主導臨床試験(先進医療Bおよび患者申出療養を除く) | あり | あり | 医師・研究者 | なし※4 | 試験により患者負担あり※6 |
| 最良の使い方を確立する試験 | 臨床試験以外 | なし | なし (すべて通常の保険診療扱い) |
健康保険一部負担分(1~3割負担) | |||
※6 医師や研究者の研究費から補填される場合がある。
臨床試験の3段階について
臨床試験には、安全性や有効性を順番に確認していく3つの段階があります。第Ⅰ相よりも第Ⅱ相、第Ⅱ相よりも第Ⅲ相のほうが治療法の開発が進んだ段階にあり、より臨床現場に近い状況にあります。
- 第Ⅰ相(フェーズ1): 少数の患者を対象に、安全性や適切な投与方法・投与量、毒性(副作用)を調べる実用化の初期段階
- 第Ⅱ相(フェーズ2): 対象を広げ、第Ⅰ相で有効で安全と判断した投与方法を用い、薬の安全性と有効性をより詳しく確認する段階
- 第Ⅲ相(フェーズ3): 多数の患者を対象に、現在の標準治療と比べて安全性や有効性の面で優れているかどうかをランダム化比較試験で確認する最終段階。
第Ⅲ相は、第Ⅰ相・第Ⅱ相を経て安全性・有効性のデータが一定程度蓄積されているため、
実用化(標準治療としての普及)まであと一歩の、最も実証データが揃っている段階の医療と言えます。そのため参加を検討しやすい選択肢となる場合があります。
第Ⅲ相試験に含まれる試験は以下の通りです。
- 主たる治験
- 医師主導治験(大規模な比較試験の場合)
- 医師・研究者主導臨床試験(大規模な比較試験の場合)
- 先進医療B
- 国際共同臨床試験(大規模な比較試験の場合)
一方で、注意点として以下の点が挙げられます。
第Ⅲ相(ランダム化比較試験)では、治療効果を客観的に評価するため、
新しい治療法の試験グループと、従来の治療法(標準治療)のグループに
無作為(ランダム)に分けて試験を実施します。
つまり、参加でき新しい薬や治療法を希望したとしても、新しい治療法を必ず受けられるという保証はありません。
費用について
前述の「保険外併用療養費制度」のお話と重なりますが、「研究段階の医療」を受ける際の費用について、「研究段階の医療」行為そのものの費用と、「研究段階の医療」以外の費用の2つに分けて考えましょう。
- 基礎的部分:診察、検査、入院料など、通常の治療と共通する部分。
保険適用で自己負担は1~3割。 - 上乗せ部分:研究のために行われる特別な検査や、まだ承認されていない
「試験薬(薬剤)」の費用。保険適用外となり全て自己負担。
「患者負担無し」のものは、製薬会社が将来の利益のためにデータを集める必要があるため、試験薬や特別な検査の費用は製薬会社が負担する場合が多いです。
「患者負担有り」のものは、原則として通常全額自己負担となります。特に患者申出療養は、未承認薬の代金だけでなく研究を管理する人件費なども含まれるため、費用が高額になる可能性があります。
試験によっては、研究費の一部を研究者が負担する場合もあれば、患者側が全額負担する場合もあります。製薬企業から薬が無償提供されるかどうかも、試験ごとに異なります。
以下には、傾向として上乗せ部分の費用負担が高額になる可能性が高い順に整理しました。
- 患者申出療養(最も高額になる可能性が高い)
患者さんの申出を起点とするこの制度は、未承認薬等の代金だけでなく、
以下の費用も全額自己負担となるため、費用が数百万単位など多額になる可能性があります。
・高額な未承認薬の代金
・データを作成するための費用:保険収載(保険適用)を目指すための厳格なデータ管理が必要であり、研究支援者の人件費、品質管理費、統計解析費などが該当 - 先進医療A
通常、全額自己負担となります。
- 拡大治験、医師主導治験、先進医療B、医師・研究者主導臨床試験
これらは試験(ケース)によって負担が変わりますが、患者負担が発生する可能性があります。
・拡大治験:製薬企業が最終的な負担を決定し、患者に一部負担を求める場合あり。
・医師主導治験:医師と患者の負担となる。製薬企業から治験薬が「無償提供」されるかどうかが費用の分かれ目。
・先進医療B:医師・研究者からの研究費の補填の有無が費用の分かれ目。
・医師・研究者主導臨床試験:承認済みの薬の組み合わせ試験であれば通常の健康保険の一部負担で済むが、希少なケースで未承認薬を用いる場合、医師・研究者からの研究費の補填の有無が費用の分かれ目。 - 企業治験・主たる治験(患者負担が最も少ない)
製薬企業が国の承認を得るために主導する試験です。
・患者負担なし:研究にかかる特別な検査や薬剤(試験薬)の費用は、製薬企業が負担
・ただし、試験薬以外の点滴代や入院料などの「基礎的部分」については通常の健康保険の自己負担は発生
「研究段階の医療」は一定のリスクを伴うことを理解しましょう
研究段階の医療は、予期せぬ副作用が起こったり、期待したような効果がみられないこともあります。さらに、標準治療においても同様のことが言えますが、同じ治療を受けても効果がある人とそうでない人がいます。
研究段階の新しい治療法によって利益が得られる可能性がある一方で、不利益を被る可能性があることも十分に理解しておくことが必要です。
また、研究段階の医療を希望する場合は、担当医や医療スタッフからの説明を理解し、十分に納得した上で、参加に同意する必要があります。
なお、同意書に署名した後や、研究段階の医療(試験)が始まる直前、すでに試験が始まっている場合でも、理由を問わずにやめることができます。
やめることを検討したい時には、担当医に相談しましょう。
(引用元:2)研究への参加はリスクを伴いますーがん情報サービス一部改変)
公的制度の検討プロセス
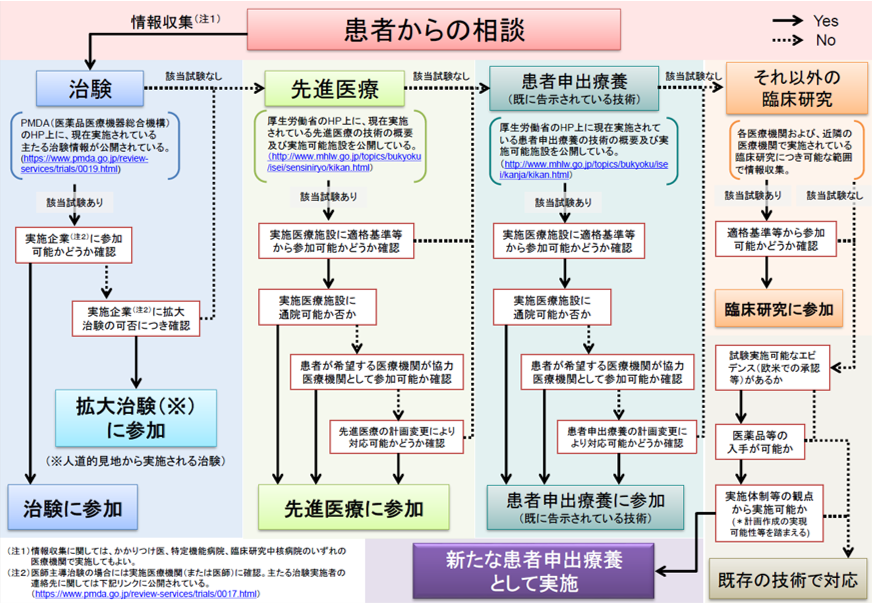
(引用元:患者申出療養までのプロセスー厚生労働省)
公的制度を実際に検討していくにあたり、厚生労働省が発信している公的制度の検討プロセスをベースにステップごとに整理していきたいと思います。
それに先立ち、まずは臨床試験の検索に活用できるサイトをご紹介します。
臨床試験の検索サイト6選
以下のサイトが公的な検索先の一例です。
- 国立がん研究センター
「がんの臨床試験を探す」:がんの種類・都道府県・実施状況などで絞り込める。チャット形式での検索機能も備わっている
(https://ganjoho.jp/public/dia_tre/clinical_trial/search2.html) - PMDA(医薬品医療機器総合機構)
「治験情報の公開」:現在実施されている主たる治験、拡大治験の情報が公開されている
(https://www.pmda.go.jp/review-services/trials/0019.html)
「治験届出者の連絡先一覧」:治験実施者の連絡先
(https://www.pmda.go.jp/review-services/trials/0017.html) - 厚生労働省
「当該技術を実施可能とする医療機関の要件一覧及び先進医療を実施している医療機関の一覧等について」:現在実施されている先進医療の技術の概要及び実施可能施設を公開している。
(https://www.mhlw.go.jp/topics/bukyoku/isei/sensiniryo/kikan.html) - 厚生労働省
「当該技術を実施可能とする医療機関の要件一覧及び患者申出療養を実施している医療機関の一覧等について」:現在実施されている患者申出療養の技術の概要及び実施可能施設を公開している。
(https://www.mhlw.go.jp/topics/bukyoku/isei/kanja/kikan.html) - 厚生労働省
「臨床研究情報ポータルサイト」:国内の主要な登録システムであるjRCT(臨床研究実施計画・研究概要公開システム)や、UMINセンター(大学病院医療情報ネットワーク)に登録された治験・臨床研究を横断的に検索できる
(https://rctportal.mhlw.go.jp/)
- がん情報サイト「オンコロ」:患者目線でわかりやすく整理されており、がん種別・部位別での絞り込みが可能
(https://oncolo.jp/ct)
【ステップ1】:担当医への相談がすべての起点になります
 どの選択肢を検討する場合においても、最初の一歩は担当医への相談です。
どの選択肢を検討する場合においても、最初の一歩は担当医への相談です。
どの臨床試験や制度が利用可能であるかは、患者さんの全身状態・治療歴・病状によって細かく決まります。担当医の判断と協力なしには、適切な選択肢にたどり着けません。
「言いにくい」と感じることもあるかと思いますが、担当医は最もよく状態を把握している協力者です。積極的に相談することで、次のステップへの扉が開きます。
以下のような質問を事前にメモしておくと、診察室での会話がスムーズになります。
また、併行して次ステップ以降の検討していく中で、気になる試験を見つけた場合、
そのWebページを印刷またはスマートフォンで写真を撮り、持参することが有効です。
- 「参加できそうな臨床試験や治験はありますか?」→ステップ2
- 「拡大治験(人道的見地からの治験)の対象になれる可能性はありますか?」
- 「先進医療として実施されている治療はありますか?、受けられる可能性のある先進医療はありますか?その病院の所在地も教えていただきたいです。」
- 「患者申出療養制度を使える可能性はあるでしょうか?」
- 「セカンドオピニオンを検討したいのですが、よろしいですか?」
【ステップ2】:「主たる治験」を確認する
研究段階で複数行われる治験のうち、安全性や有効性を確認する最終段階のものを指します。通常は、効能・効果および用法・用量が一連の開発を通じて設定された後に、安全性および有効性の検証を目的として行われているものです。
そのため、第Ⅰ相・第Ⅱ相を経て安全性・有効性のデータが一定程度蓄積されているため、参加を検討しやすい選択肢ともいえます。
「第Ⅲ相」や「主たる治験」という言葉が出てきたら、それは「実用化(標準治療としての普及)まであと一歩の、最も実証データが揃っている段階の医療」として、優先順位の高い検討候補とご認識いただければと思います。
PMDA(医薬品医療機器総合機構)のホームページ上に、現在実施されている主たる治験情報が公開されています。
(引用元:治験情報の公開ーPMDA)
(引用元:治験届出者連絡先一覧ーPMDA)
患者さん自身では直接申し込めず段取りを組めないため、担当医に以下のように相談すると良いかと思います。
- 「この病院で参加できそうな(主たる)治験を探してほしい、候補があれば実施企業に参加可能か確認してほしい」
- 「他の病院で実施している(主たる)治験を探してもらえるか、候補があれば実施企業とその病院に参加可能か確認してもらえるか、その病院に紹介してもらえるか又はこの病院で実施可能か」
- 「自分で探して見つけてきた(主たる)治験について参加可能か確認してほしい、可能性があれば実施企業と実施医療機関への確認や参加までの段取りを組んでもらえるか」
【ステップ3】:主たる治験の参加基準を満たせない場合は「拡大治験」を確認する
ステップ2で見つけた試験の参加条件(年齢・病状・治療歴など)に合わなかった場合も、「拡大治験(人道的見地から実施される治験)」という選択肢があります。
この制度は2016年1月に正式に制度化されました。通常の治験の枠に入れない患者さんに対して、人道的な観点から未承認薬へのアクセスを認めるものです。
拡大治験を利用するには、以下の3つの条件をすべて満たす必要があります。
~拡大治験の対象条件~
- 生命に重大な影響がある疾患であること
- 既存の治療法に有効なものが存在しないこと
- 対象薬剤が「主たる治験」の実施後または組入れ終了後にあること
現在実施されている主たる拡大治験情報についても、PMDA(医薬品医療機器総合機構)のホームページ上に公開されています。
(https://www.pmda.go.jp/review-services/trials/0019.html)
(治験届出者連絡先一覧:https://www.pmda.go.jp/review-services/trials/0017.html)
実施できる医療機関は「主たる治験」を実施した・している施設に限られます。
こちらも以下のように相談すると良いかと思います。
- 「(希望の主たる治験に参加できなかったため)拡大治験に参加可能か、実施企業に確認してほしい」
- 「他の病院で実施している拡大治験を探してもらえるか、候補があれば実施企業とその病院に参加可能か確認してもらえるか、その病院に紹介してもらえるか」
- 「自分で探して見つけてきた拡大治験について参加可能か確認してほしい、可能性があれば実施企業と実施医療機関への確認や参加までの段取りを組んでもらえるか」
【ステップ4】:認められた医療機関で実施中の「先進医療」を調べる
先進医療とは、厚生労働省が指定した医療技術のうち、将来的な保険収載を目指して有効性・安全性を評価している段階にある技術です。
先進医療には「先進医療A」(未承認薬等を用いない治療法)と「先進医療B」(未承認・評価が必要な治療法)の2種類があります。(「専門用語まとめ」参照)
厚生労働省のホームページ上に、現在実施されている先進医療の技術の概要及び実施可能施設が公開されています。
(引用元:先進医療を実施している医療機関の一覧等についてー厚生労働省)
技術ごとに一定の施設基準が設けられ、届け出が必要になることから、実施できる医療機関はかなり限定されます。
そのため、誰でも・どこでも受けられるわけではありませんので、
こちらも以下のように相談すると良いかと思います。
- 「参加できる先進医療があるか確認してほしい、(通院可能であれば)実施医療機関に適格基準等から参加可能か確認してほしい」
- 「(通院が難しければ)この病院又は希望する病院が協力医療機関として参加可能か確認してほしい」
- 「(望みは薄いかも分からないが)先進医療の計画変更により対応可能かどうか確認してほしい」
- 「自分で探して見つけてきた先進医療について参加可能か確認してほしい、可能性があれば参加までの段取りを組んでもらえるか」
【ステップ5】:患者さんの申出を起点とする「患者申出療養制度」を活用する
治験・拡大治験・先進医療のいずれにも該当する選択肢が見つからなかった場合の最後の公的制度が、「患者申出療養制度」です。患者さん自身の「受けたい」という申出を起点として、将来の保険適用を目指すためのデータを集めながら、未承認薬などの治療を国内で受けられる仕組みで、2016年4月にスタートした制度です。
【既に前例がある医療を希望する場合】
すでに患者申出療養として実施された実績があり、国から告示されている治療法を希望する場合です。
- 担当医への相談
まずは今の病状にその治療が適しているか、担当医と相談します。 - 前例を取り扱った病院への照会(担当医が実施)
担当医が、その前例を実施した臨床研究中核病院に設置されている患者申出療養に関する専用窓口(臨床研究中核病院及び特定機能病院に係る患者申出療養相談窓口設置状況一覧表ー厚生労働省)に連絡し、担当医に診てもらっている当院、または身近な医療機関で実施できるのか、実施可能性を確認します。 - 臨床研究中核病院への申出(実質は担当医が実施)
医学的な調整が整った段階で、患者さんから(担当医経由で)臨床研究中核病院に対して申出を行います。(臨床研究中核病院には担当医から申し込みができるフォームが設けられています。)
- 病院間での連携・事務手続き(申出後、原則2週間)
国による個別の審議は不要であり、臨床研究中核病院が、担当医に診てもらっている当院、または身近な医療機関の実施体制を個別に審査します。ほとんどが事務的な処理のみであるため迅速に進められます。 - 担当医に診てもらっている当院、または身近な医療機関での治療開始
なお、現在通院している病院(担当医に診てもらっている当院)が臨床研究中核病院であり、実施された前例がある場合は、さらに手続きがスムーズになることが想定されます。
【前例のない「初めての医療」を希望する場合】
患者申出療養として実施されたことがない新しい治療法を希望する場合です。国の審議会で慎重に審査されるため、開始までには一定の時間がかかります。
- 担当医への相談
まずは今の病状にその治療が適しているか、担当医と相談します。
- 専門窓口への照会(担当医が実施)
担当医から、臨床研究中核病院または特定機能病院に設置されている患者申出療養に関する専用窓口(臨床研究中核病院及び特定機能病院に係る患者申出療養相談窓口設置状況一覧表ー厚生労働省)へ相談・調整を依頼します。 - 実施計画の作成(臨床研究中核病院が実施)
窓口経由で相談内容が検討され、最終的に臨床研究中核病院が、実施中の治験、先進医療B、拡大治験では申出のあった医療技術を受けられないことを確認します。
将来の保険収載を見据えた実施計画書や、患者申出療養に係る申出書などの必要書類を作成し、協力医療機関として、担当医に診てもらっている当院、または身近な医療機関を申請をしてもらいます。
また、製薬企業に未承認薬・適応外薬の手配を依頼する場合も臨床研究中核病院等が代行します。
- 国(厚生労働省)への申出(実質は担当医が実施)
臨床研究中核病院が作成した書類を添えて、患者さんから(担当医経由で)国に対して正式な申出を行います。 - 国の審議会による審査(申出後、原則6週間)
患者申出療養評価会議にて、安全性や有効性、計画の妥当性が審査されます。医学的判断が分かれるなど、6週間で判断できない場合もあります。 - 担当医に診てもらっている当院、または身近な医療機関での治療開始
国から承認された後、詳しい説明を受け、同意書に署名をして治療が始まります。
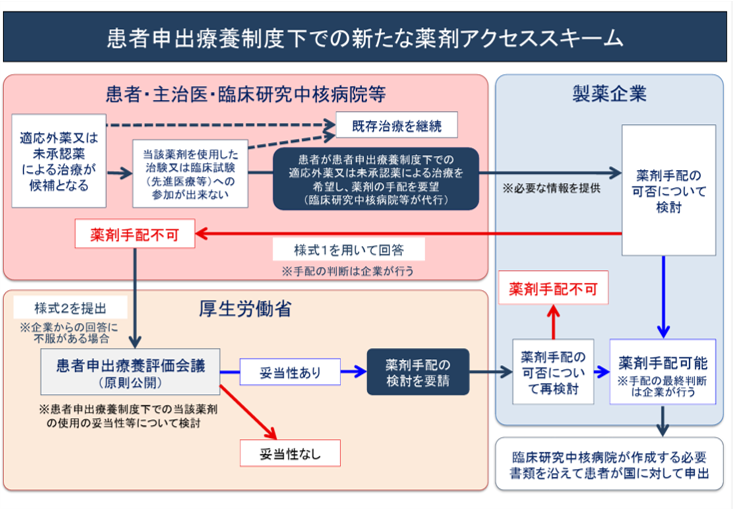
(引用元:患者申出療養制度下での薬剤アクセススキームについてー厚生労働省)
また、厚生労働省のホームページ上に、患者申出療養を実施している医療機関の一覧や現在実施されている患者申出療養の技術の概要等が公開されています。
(引用元:患者申出療養を実施している医療機関の一覧等についてー厚生労働省)
- 費用は「全額自己負担」が基本です
前述の通り、「研究部分(未承認薬の代金やデータ管理費など)」はすべて患者負担となります。薬代だけで常に高額になる可能性があるため、事前の確認が不可欠です。 - 必ず受けられるとは限りません
医学的な根拠が不十分と判断されたり、製薬企業から薬剤が提供されなかったりした場合は、申出をしても実施できないことがあります。 - 治験や先進医療が優先です
前ステップまでで先に検討してきましたが、希望する治療がすでに治験や先進医療の枠組みで実施されている場合は、まずはそちらへの参加を優先して検討することになります。(臨床研究中核病院が確認します)
【ステップ6】:エビデンスのある「補完・統合医療」を検討する
ステップ6と表記させていただきましたが、可能な範囲で前ステップのタイミングから併行していただければとより良いかと思います。

補完・統合医療は、標準治療の代わりになるものではなく
「補助的に組み合わせる」ことで副作用の軽減や生活の質(QOL)の維持を目指すものです。
重要なのは、科学的根拠(エビデンス)に着目し、必ず担当医に相談してから取り入れることです。
エビデンスが定かではない上に高い治療効果があると謳っているようなものが
広まりやすい分野でもあるため、情報の見極めが特に重要になります。
最初にチェックしてほしい情報源:eJIM(厚生労働省)
厚生労働省の統合医療情報発信サイト「eJIM(イージム)」
(https://www.ejim.mhlw.go.jp/public/index.html)では、漢方・サプリメント・各種施術などについて科学的根拠に基づいた情報を日本語で調べることができます。
また、情報の見極め方についても詳しく説明がされており、
「補完・統合医療」を検討する際の最初にチェックしてほしい情報源としてご活用いただければと思います。
以下にこのサイトでできることをまとめました。
|
カテゴリ(できること)
|
主な内容・詳細
|
主なページリンク
|
|---|---|---|
|
基礎知識を学ぶ
|
「統合医療」の定義や考え方、インターネット上の医療情報の見極め方を学べます。
|
|
|
科学的根拠(エビデンス)を調べる
|
健康食品、コクランレビュー※、国内外の臨床試験をまとめた構造化抄録などを確認できます。
|
|
|
冊子・資料を閲覧する
|
厚生労働省や国立がん研究センター等が作成した、信頼性の高いガイドラインやパンフレットを閲覧できます。
|
|
|
海外の最新情報を得る
|
米国国立補完統合衛生センター(NCCIH)が発信している、サプリメントや各種療法に関する情報の日本語訳を閲覧できます。
|
|
|
文献検索に活用する
|
世界最大の医学文献データベース「PubMed」を使い、自分で情報を検索する方法が詳しく解説されています。
|
※ コクラン・レビュー:医学論文のシステマティック・レビューを行なう国際的団体コクランが作成する質の高いシステマティック・レビューであり、世界中の論文を専門家が体系的に検証した最も信頼性の高い系統的レビュー
コクラン・レビュ・サマリー(臓器・疾患別分類)では、疾患別に日本語で一覧に整理されており、リンク先でもそのまま日本語で閲覧できるためおすすめです。
科学的根拠のある漢方薬に関する情報源:EKAT(日本東洋医学会EBM委員会)
日本東洋医学会EBM委員会が公開している「EKAT(漢方治療エビデンスレポート)」は、1986年以降に実施された漢方製剤のRCT(ランダム化比較試験)を網羅的に収集・整理したデータベースです。2025年1月時点で583件の構造化抄録が収録されており、特定のがん症状や治療副作用に対する漢方薬の効果を確認できます。
(漢方治療エビデンスレポートー日本東洋医学会EBM委員会)
(漢方製剤の記載を含む診療ガイドラインー日本東洋医学会EBM委員会)
参考までに、がん治療に関連してエビデンスが確認されている主な漢方処方は以下のとおりです。
- 六君子湯(りっくんしとう):シスプラチン等による食欲不振に対してRCTで有意な改善が確認されている
- 十全大補湯(じゅうぜんたいほとう):放射線治療後の全身倦怠感・食欲不振・悪心にRCTで有用性が示されている
- 補中益気湯(ほちゅうえっきとう):がんに伴う疲労感(倦怠感)にRCTで有効性が確認されている
- 牛車腎気丸(ごしゃじんきがん):抗がん剤(オキサリプラチン等)による末梢神経障害への使用が知られている(※ただし、オキサリプラチンについてはガイドライン上、予防としての投与は「4B 投与しないことの弱い提案、効果は否定的であるという中等度のエビデンス」との記載あり)
なお、各学会が発行する「診療ガイドライン」に漢方薬が推奨として記載されているケースも増えています。ご自身の調査に併行して担当医に確認してみると良いかと思います。
補完代替療法を取り入れる前に必ず担当医に相談する
補完代替療法は、現在受けている抗がん剤・放射線治療と相互作用を起こすリスクがあります。「天然由来物質だから安全」とは限りません。
天然由来成分の漢方治療ががん治療時の副作用軽減にエビデンスがあることも考慮しても、不適切に適用すれば悪影響が出てきても不思議ではありません。
情報を入手した後、必ず担当医に伝えて安全性を確認してから取り入れてください。
セカンドオピニオンを有効活用する
現在の担当医以外の専門医に意見を聞く「セカンドオピニオン」は、ステップ2〜6の選択肢についてより広い視野で情報を得るうえで非常に有効です。担当医に「セカンドオピニオンを受けたい」と申し出ることは、患者さんの正当な権利であり、関係が悪化することを心配する必要はありません。
特に、がんゲノム医療・希少がん・治療抵抗性のがんなど、専門性の高い領域では、専門施設でのセカンドオピニオンが新たな選択肢の発見につながることがあります。
信頼できる医療情報の探し方と見極め方
ここまで、標準治療の次の治療選択肢の検討プロセスを中心にお話してきました。
ここからは、治療の選択肢を検討する際に備えておきたいヘルスリテラシーについて解説していきます。
ヘルスリテラシーとは、「どこで情報を得るか」という情報の探し方、「その情報が信頼できるか」を見極める・判断する力のことです。
特にがん治療分野はインターネット上に根拠の乏しい情報があふれており、正しい情報源にたどり着くことが「根拠のある選択」への第一歩になります。
信頼できる情報源
前述の臨床試験の検索サイト6選に加え、以下の公的・専門的なサイトが情報の信頼性が高く、最初に参照することをおすすめします。ただし、英文サイトについては取っつきにくいかと思いますので、無理のない範囲でご活用いただければと思います。
なお、英文文献への対応方法については以下の記事もご参照いただければと思います。
医療情報の見極めに役立つ3つの方法【PC・図書館・翻訳ツール活用】
- 厚生労働省eJIM(https://www.ejim.mhlw.go.jp/public/index.html):漢方・サプリメントなどの統合医療について、エビデンスに基づく情報を日本語で発信
- 国立がん研究センター「がん情報サービス」(https://ganjoho.jp/public/index.html):国内で最も信頼性の高いがん情報のポータルサイト
- Cochrane Library(コクラン・ライブラリー)(英文)
(https://www.cochranelibrary.com/):世界中の論文を専門家が厳密に検証した「系統的レビュー」を提供する、国際的に最も権威ある情報源のひとつ
※前述の通り、厚生労働省eJIMサイト内のコクラン・レビュ・サマリー(臓器・疾患別分類)では、疾患別に日本語で一覧に整理されており、リンク先でもそのまま日本語で閲覧できるためおすすめです。
(コクラン・レビュー・サマリー:https://www.ejim.mhlw.go.jp/doc/index_cochrane.html) - 統合腫瘍学ガイドライン(英文)(https://www.ejim.mhlw.go.jp/doc/index_cochrane.html):統合腫瘍学会(Society for Integrative Oncology: SIO)が作成・提供している、標準的ながん治療に補完・統合療法を組み込むための唯一の包括的なエビデンスに基づく指針
また、最近ではAIも発達し優秀な翻訳ツールもあるかと思いますので、
より使いやすい方法がありましたら追って執筆させていただきます。
エビデンスレベルで情報の質を判断する
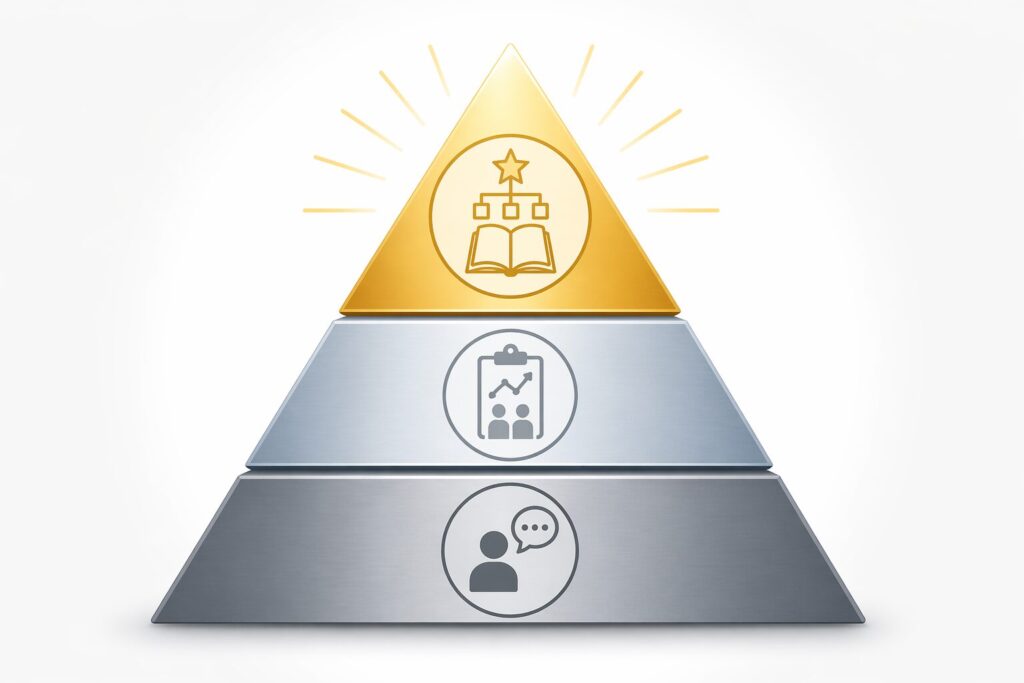
手に入れた情報の信頼性を判断するには、「研究デザイン」に注目することが有効です。以下のように、研究の種類によって信頼性のレベルが異なります。
- メタアナリシス(系統的レビュー):複数の質の高い論文を統合して分析したもの。コクラン・レビューがその代表例。現時点で得られる最も信頼性の高いエビデンス
- ランダム化比較試験(RCT):患者を無作為に2群に分けて効果を比較する試験。バイアスが少なく、科学的な質が高いとされる
- 症例報告・体験談:個人の経験に過ぎず、全員に当てはまるとは言えないため、科学的証明としての価値は最も低い
「この治療で治った」という体験談は強く印象に残りますが、症例報告はあくまでも個人の事例です。治療法を選ぶ際の根拠としては不十分である点に注意しましょう。
粗悪な療法を見分ける4つのレッドフラッグ
非常に残念なことですが、がん治療中であらゆる標準治療が奏功せず、藁にもすがる思いで治療法を探す患者さんやそのご家族の気持ちを無視したものが多数存在します。
以下のような特徴がある情報や療法には、特に注意が必要です。
- 断定的な表現:「がんは〇〇で治る」「免疫力が上がる」のように、科学的根拠を明記せずに断定的な表現が使われている
- 体験談に偏っている:論文・研究データの提示がなく、個人の感想のみが強調されている
- 高額な全額自己負担:「自由診療」として高額な費用を請求し、保険診療との併用が認められない
(前述の内容から、評価療養、患者申出療養以外で高額な療法に手を出すリスクは計り知れないことがお分かりいただけるかと思います。) - 担当医への秘密:「医師には内緒で」「病院の治療と並行してこっそり試してほしい」といった言い方をする
個人的な意見ですが、高額な負担もいとわないとお決めになられた際は、
聞いたことのないものでなく、患者申出療養にかけた方が良い方向に向かう可能性は高いと考えております。
PubMedで論文を読む際のポイント
世界最大の医学論文データベース「PubMed」(https://pubmed.ncbi.nlm.nih.gov/)では、最新の研究結果を確認できます。専門的ですが、以下の点に注目すると読みやすくなります。
- 構造化抄録(Abstract):目的・方法・結果・結論が整理されており、全文を読まなくても概要を把握できる
- 副作用(Adverse events / Safety)の記載:メリットだけでなく、リスクや副作用についても誠実に記載されているかを確認する
- サンプルサイズと追跡期間:対象人数が少なすぎる・追跡期間が短すぎる研究は、結論を一般化できない可能性がある
(前述の通り、メタアナリシス(Meta-Analysis)やランダム化比較試験(Randomized Controlled Trial)でフィルタリングがおすすめです)
PubMedで見つけた論文は、必ず担当医に見せて解釈を確認することをおすすめします。論文の読み方や結果の解釈には専門知識が必要なため、情報収集の参考として活用しましょう。
前述しましたが、PubMedの使い方などは以下の情報をご参照いただければと思います。
インパクトファクター(Impact Factor)とは、
学術雑誌(ジャーナル)の影響度を評価する指標のことです。同じ分野の雑誌同士を定量的に比較するための手段として、世界的に活用されています。
専用のデータベース「Journal Citation Reports」(https://jcr.clarivate.com/)で確認することができますが、有料ツールとなりますので、
多くの場合は大学附属図書館の学内ネットワークを利用することになるかと思います。
気になる英文論文が有料であった場合にも大学附属図書館からのアクセスで閲覧できる場合もありますので、近隣に大学附属図書館がある場合はホームページやサポート窓口に確認いただければと思います。
クラリベイト・アナリティクス社のデータベース「Web of Science」を元に毎年算出され、数値が高いほど、その雑誌に掲載された論文が他の論文に多く引用されている(=影響力が大きい)とみなされます。
- 異分野間での比較はできない: 分野によって論文を引用する慣習(引用数や頻度)が大きく異なるため、専門分野が違う雑誌同士の比較には活用できません。
- 個々の論文や研究者の評価ではない: インパクトファクターはあくまで「雑誌全体」に与えられるものです。その雑誌に載ったからといって、個別の論文の質や研究者の能力を直接的に表したものではありません。
- 引用数以外の性質は分からない: あくまで引用された回数を元にした指標であり、論文の内容の良し悪しや雑誌の専門的な性質までは表現できません。
まとめ:納得のいく判断のために
標準治療が奏功しなかった場合でも「治療の終わり」ということではなく、研究段階の医療という可能性が残されています。
標準治療とは異なり患者さん側からのアプローチが必要となる一方で、その膨大な情報量や判断の難しさが相まって、これら制度を十分に活用できないケースや治癒の可能性があったかもしれないケースが多いと推察されます。
最も安全でリスクの低い方法は、
「公的な制度から順番に検討し、担当医に相談する」というサイクルを繰り返しながら、可能な範囲でご自身でも信頼できる情報源で根拠を確認し納得できることです。
以下にこの記事でお伝えした内容をまとめます。
- ステップ1:担当医への相談(全ての起点)
- ステップ2:「主たる治験」を確認する
- ステップ3:参加基準を満たせない場合は「拡大治験」を確認する
- ステップ4:認められた医療機関で実施中の「先進医療」を調べる
- ステップ5:「患者申出療養制度」を活用する
- ステップ6:eJIM・EKATでエビデンスを確認した上で「補完・統合医療」を検討する
費用の面では、評価療養(治験・先進医療)や患者申出療養は「保険外併用療養費制度」の枠組みにより、診察・検査・入院料等の基礎的部分に保険が適用されます。
研究段階の医療の費用(試験薬など)は原則自己負担となりますが、企業・主たる治験は製薬企業が負担するケースが多く、患者負担が最も少なくなります。
信頼できる情報を得るため、公的・専門的なサイト(eJIM、がん情報サービス、jRCT、PMDA、コクラン・ライブラリーなど)を第一の情報源としてご活用ください。
体験談よりもランダム化比較試験(RCT)やシステマティックレビューを重視し、粗悪な療法の4つのレッドフラッグ(断定的表現・体験談偏重・高額自由診療・担当医への秘密)を意識することで、情報に惑わされない正当な判断の一助になるかと思います。
患者さんご本人やご家族のより良い選択のために、この記事が少しでも役に立っていただければ幸いです。
これからも皆さんの日々の生活が『より良く』なるような情報を発信していきます。
以上、ぐぅでした。
※本記事の画像はAI生成(NotebookLM、ChartGPT)です。